Mikronährstofftherapie
| Definition |
|
Bei der Koronaren Herzkrankheit (KHK) handelt es sich um eine chronische, atherosklerotische und entzündliche Erkrankung des Herzens, welche sich durch stabile Angina, instabile Angina, Myokardinfarkt (MI) oder plötzlichen Herztod manifestiert. Die KHK zählt zu den wichtigsten Herz-Kreislauf-Erkrankungen und stellt in vielen Teilen der Welt die häufigste Todesursache dar. Um die verschiedenen Aspekte dieser Erkrankung zu verstehen wurden mehrere Konsortien, Fall-Kontroll-Studien, epidemiologische Studien und genomweite Assoziationsanalysen (GWAS) durchgeführt. Zu den Risikofaktoren der KHK gehören neben Diabetes mellitus, Bluthochdruck, Rauchen auch Hyperlipidämie, Fettleibigkeit, Homocystinurie und psychosozialer Stress. Darüber hinaus wurde festgestellt, dass der Lebensstil eine wichtige Rolle bei der Entstehung solcher Herz-Kreislauf-Erkrankungen spielt. Das Verständnis der mit der KHK verbundenen Risikofaktoren, die Annahme einer gesunden Lebensweise und präventiver Strategien sowie eine frühzeitige Diagnose haben in den letzten Jahrzehnten wesentlich zur Verbesserung und Prognose von Patienten, die an einer KHK oder einer anderen Herz-Kreislauf-Erkrankung leiden, beigetragen. |
| Ursachen und Symptomatik |
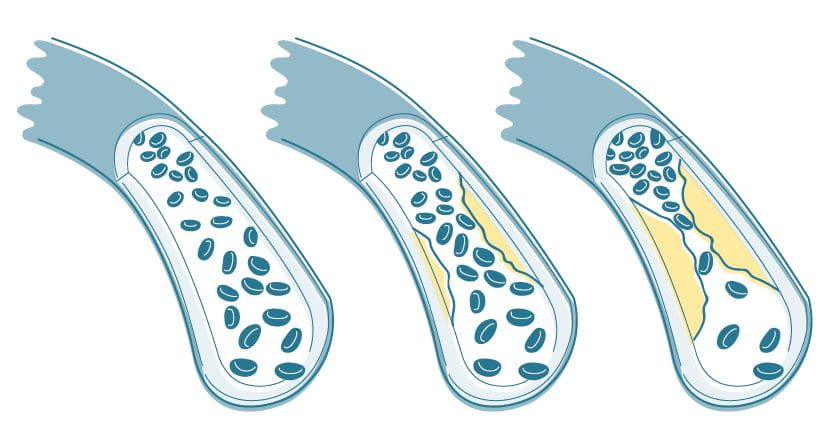
| Die KHK ist eine kardiovaskuläre Erkrankung, die durch Atherosklerose oder atherosklerotische Verschlüsse der Koronararterien entsteht. Wenn die Endothelfunktion der Arterienwand gestört ist, beginnt die Atherosklerose aufgrund der Ansammlung von Lipoproteintröpfchen in der Intima der Koronargefäße. Im Blutkreislauf zirkulieren wasserunlösliche Lipide, indem sie sich an wasserlösliche Lipoproteine, die Apolipoproteine genannt werden, anlagern. Low-Density-Lipoproteine (LDL) besitzen in hoher Konzentration die Fähigkeit, das gestörte Endothel zu durchdringen und sich einer Oxidation zu unterziehen. Dieses oxidierte LDL lockt dann Leukozyten in die Intima der Herzkranzgefäße, die von Makrophagen aufgespült werden können, was zur Bildung von Schaumzellen führt. Diese schaumigen Zellen replizieren sich und bilden Läsionen, die als Fettstreifen bezeichnet werden. Dies ist die früheste Form von Läsionen, die bei der Atherosklerose sichtbar werden. Die Bildung solcher Läsionen löst Signale aus, die glatte Muskelzellen (engl. Smooth Muscle Cells, SMCs) an die Stelle des Fettstreifens locken. Die SMCs beginnen anschließend mit der Proliferation und Produktion von extrazellulärer Matrix, hauptsächlich Kollagen und Proteoglykanen. Die atherosklerotische Plaque beginnt sich zu entwickeln und akkumuliert ein großes Volumen an extrazellulärer Matrix, die von den SMCs produziert wird, was zur Progression der Läsion zu faseriger Plaque führt. Die faserige Plaque dringt in das Lumen des Herzkranzgefäßes ein und es bilden sich kleine Blutgefäße, die anschließend die Plaques verkalken können. Die schließlich gebildete Läsion ist eine fortgeschrittene und komplizierte Läsion, die aus einer faserigen Kappe mit einem darüber liegenden lipidreichen Kern besteht, der nekrotisches Material enthält, das stark thrombogen sein kann. Die von den SMCs produzierten Proteoglykane können sich an Lipoproteine binden und deren Existenz in der Intima verlängern, wodurch sie anfällig für oxidative Modifikationen und nicht enzymatische Konjugation mit Zuckern, auch Glykation genannt, sind. Die modifizierten Lipoproteine, nämlich oxidierte Phospholipide und fortgeschrittene Glykierungsendprodukte, können Entzündungsreaktionen propagieren. Matrix-Metalloproteinasen (MMPs) werden von den Endothelzellen als Reaktion auf Oxidation, hämodynamische, entzündliche und Autoimmun-Signale abgesondert. Diese MMPs, zusammen mit einem Gleichgewicht ihrer körpereigenen Gewebeinhibitoren, modulieren verschiedene Funktionen der Gefäßzellen, wie Aktivierung, Migration, Proliferation, Zelltod, geometrische Umgestaltung, Gefäßneubildung, Zerstörung der extrazellulären Matrix der Arterien und des Myokards und Heilung. In den atherosklerotischen Läsionen kommt es häufig zum Zelltod oder zur Apoptose, was schließlich zur Ablagerung des Gewebefaktors in partikulärer Form führt. Als Folge der Bildung der atherosklerotischen Plaque in der Koronararterie kommt es zu einer Behinderung des Blutflusses, was zu einem Missverhältnis zwischen myokardialem Sauerstoffbedarf und -angebot führt. Diese Obstruktion manifestiert die Symptome der KHK, wie z.B. unterseitige Beschwerden, Schweregefühl, ein druckähnliches Gefühl, das in den Kiefer, die Schulter, den Rücken oder den Arm ausstrahlen kann. Diese Symptome dauern in der Regel mehrere Minuten an und werden normalerweise durch eine schwere Mahlzeit, emotionalen Stress, Anstrengung oder Kälte hervorgerufen. Innerhalb von Minuten können diese Symptome durch Ruhe oder Nitroglyzerin gelindert werden. |
| Risikofaktoren, welche mit einer KHK assoziiert sind |
|
Die Risikofaktoren, die mit der Entwicklung der KHK verbunden sind, wurden durch umfangreiche epidemiologische Forschung ermittelt und umfassen Rauchen, Diabetes, Hyperlipidämie und Bluthochdruck. Fall-Kontroll-Studien und Kohortenstudien mit 20 Millionen Menschen machten deutlich, dass bei Rauchern 70 % mehr Todesfälle durch KHK auftreten als bei Nichtrauchern. Rauchen hat Einfluss auf die atherosklerotische Läsion und fördert auch den Koronarverschluss, da es eine endotheliale Denudation und die Anhaftung von Thrombozyten an subintimale Schichten erzeugt, wodurch die Lipidinfiltration und die durch den Thrombozytenwachstumsfaktor (PDGF) vermittelte Proliferation von SMCs erhöht wird. Diabetes, insbesondere Diabetes mellitus oder Typ-2-Diabetes, stellt einen Risikofaktor für KHK dar. Es wurde beobachtet, dass Diabetes häufig mit Hyperlipidämie assoziiert ist, die durch erhöhte Triglyceridwerte und verringerte HDL-Cholesterinwerte gekennzeichnet ist. Niedrige Werte von HDL-Cholesterin, hohe Werte von sehr niedrigem Lipoprotein (VLDL)-Cholesterin und hohe Werte der gesamten VLDL-Triglyceride wurden als Risikofaktoren für KHK bei Patienten mit Typ-2-Diabetes berichtet. In der PROCAM (Prospective Cardiovascular Münster Study)-Studie wurde eine starke Assoziation zwischen Bluthochdruck und KHK berichtet, was auf die Prävalenz von Hypertonie bei Patienten mit Myokardinfarkt in einer Nachbeobachtung von 4 Jahren schließen lässt. Es besteht ein pathophysiologischer Zusammenhang zwischen Hypertonie und KHK, da die Atherosklerose durch die arterielle Hypertonie verschlimmert werden könnte. Durch die Ablagerung von Lipiden und die Bildung von atherosklerotischen Plaques in den Arterien steigt der transmurale Druck in den Arterien. Er übt eine zunehmende mechanische Belastung und endotheliale Permeabilität aus und trägt so zu einer Abnahme der koronaren Reaktion bei. Bluthochdruck wurde auch häufig mit Stoffwechselstörungen wie Insulinresistenz oder Hyperinsulinämie und Dyslipidämie in Verbindung gebracht, die auch als Risikofaktoren für KHK bekannt sind. Hyperurikämie wird im Allgemeinen definiert als der Überschuss der im Körper vorhandenen Serum-Urat-Konzentration. Die Serum-Harnsäure ist das Produkt des Purin-Stoffwechsels, das in einer Konzentration von mehr als 6,8 mg/dl eine Hyperurikämie verursacht. Studien haben auf einen Zusammenhang zwischen Hyperurikämie und dem Risiko einer KHK hingewiesen. Stress ist als wichtiger und potenziell veränderbarer Risikofaktor für Herz-Kreislauf-Erkrankungen anerkannt. Verschiedene physiologische Veränderungen, die durch Stress hervorgerufen werden, können für Herz-Kreislauf-Erkrankungen relevant sein. Zu solchen Reaktionen gehören erhöhter Blutdruck, verminderte Insulinsensitivität, erhöhte Hämostase und endotheliale Dysfunktion. Psychosozialer Stress mit beruflicher Belastung hat sich ebenfalls als Risikofaktor der KHK erwiesen. In einer Fall-Kontroll-Studie von INTERHEART wurde berichtet, dass die berufliche Belastung bei Männern mit einem höheren Myokardinfarkt-Risiko verbunden ist als bei Frauen. |
| Diagnostik |
|
Bei der Diagnose einer KHK steht in erster Linie die Anamnese durch den behandelnen Arzt mit anschließender körperlicher Untersuchung im Vordergrund. Als weiterführende Diagnostik können sowohl invasive (u.a. Koronarangiographie, Koronarangioskopie) als auch nicht-invasive Verfahren (u.a. Ruhe- und Belastungs-EKG, Echokardiografie, MRT) dienen. In der Prävention einer KHK steht die Erkennung der Risikofaktoren mit gleichzeitiger Minimierung dieser. Einen wesentlichen Beitrag dazu kann die labordiagnostische Analyse von Parametern und Risikomarkern liefern, welche in direkter Weise mit dieser Erkrankung in Verbindung stehen. Mithilfe des ultrasenstiven CRPs können chronische Entzündungen in den Gefäßen erkannt werden, da dieser als unabhängiger Marker zur Früherkennung agiert, wenn keine weiteren Risikofaktoren erkennbar sind. Die Bestimmung des ultrasensitiven CRPs unterstützt bei Patienten mit unauffälligen Plasmalipidwerten die Abschätzung des kardiovaskulären Risikos, da dieser den aktuellen Grad der Entzündung in den Gefäßwänden wiederspiegelt. Erhöhtes ultrasensitives CRP steht mit einem höheren Risiko für koronare Herzkrankheiten und periphere Arterienerkrankungen in Zusammenhang. Während Werte < 0,7 mg/l ein geringes Risiko aufzeigen, deuten Werte von > 5,0 mg/l auf ein akutes, entzündliches Geschehen bzw. Werte > 1,9 mg/l auf ein hohes kardiovaskuläres Risiko hin. Im extravaskulären Raum der Gefäßwände kann LDL oxidiert werden. Aufgrund der höheren Konzentrationen von Antioxidantien ist es in der Zirkulation davor weitgehend geschützt. Oxidiertes LDL weist ein hohes atherogenes Potenzial auf und kann dadurch in den Gefäßwänden Low-grade Entzündungen auslösen. Die Bestimmung des Wertes kann somit zur Beurteilung von Progression und Prognose atherosklerotischer Plaques eingesetzt werden. Des Weiteren steht das oxidierte LDL in Verdacht die Bildung von Triglyceriden zu fördern und folglich die Fetteinlagerung zu steigern, das wiederum die Bildung von oxidiertem LDL verstärkt. Physiologisch sind weniger als 1% des im Blut zirkulierenden LDL oxidativ verändert, Werte >235 ng/ml zeigen ein erhöhtes Risiko auf. Folglich wird dadurch die Ausschüttung von Adhäsionsmolekülen und Zytokinen stimuliert, was eine Auslösung weiterer Entzündungsprozesse zur Folge haben kann. Lp-PLA2 erweist sich als wichtiger Prädiktor zur Abschätzung des Risikos, weil das Enzym verstärkt in den zur Ruptur neigenden instabilen Plaques nachgewiesen werden kann. Labordiagnostisch lässt sich im PLAC®-Test die Aktivität der Lp-PLA2 ermitteln, welche als spezifischer Marker für vaskuläre Entzündungen dient, da bei systemischen Entzündungen keine erhöhten Werte auftreten. Das koronare Risiko gilt über einem kritischen Aktivitätswert von 507 U/l bei Frauen und 639 U/l bei Männern als erhöht. Bei der vaskulären Kalzifizierung (Gefäßverkalkung) handelt sich um ein weit verbreitetes Merkmal der Arterioskerlose, des Alterns und der Diabetes mellitus und wird zusätzlich mit einem gehäuften Auftreten von Herz-Kreislauferkrankungen assoziiert. Das Matrix γ-Carboxyglutaminsäure (GLA)-enthaltendes Protein (MGP) agiert als wichtiger, lokaler Inhibitor der Gefäßverkalkung, allerdings erst nach Aktivierung durch eine Vitamin K2-abhängige Carboxylierungsreaktion. Bei Vorliegen eines Vitamin K2-Mangels steigt der Spiegel an uncarboxyliertem, inaktiven MGP (dp-ucMGP) an, wodurch die Entstehung von Artherosklerose begünstigt wird. Ein erniedrigter Vitamin K2-Gehalt kann nicht nur alimentär bedingt sein, sondern auch durch die wiederholte Einnahme von Antibiotika, Salicylaten, Vitamin K-Antagonisten sowie Alkoholismus und Leber- und chronische Magen-Darmerkrankungen verursacht werden. Eine Erhöhung des inaktiven, uncarboxylierten MGP (dp-ucMGP) dient somit als Hinweis auf eine unzureichende Vitamin K2-Versorgung und agiert zusätzlich als sensitiver Marker für vaskuläre Kalzifizierungen und kardiovaskuläre Erkrankungen. Das Enzym Myeloperoxidase (MPO) wird überwiegend von aktivierten Granulozyten freigesetzt und ist in den Abwehrprozess von Mikroorganismen involviert. Zusätzlich können Granulozyten auf den Kontakt mit Cholesterin in den Gefäßwänden mit der Bildung von MPO reagieren, was wiederum zur Entstehung von Schaumzellen beiträgt und in weiterer Folge die „Verkalkung“ des Gefäßes vorantreibt. Des Weiteren verfügt MPO über oxidative und pro-inflammatorische Eigenschaften, welche zu einer Beeinträchtigung der Endothelfunkiton führen können, weswegen dem Enzym eine zentrale Rolle bei der Entstehung koronarer Herzerkrankungen zugeschrieben wird. Studien zufolge weist sich MPO als geeigneter Marker in der Diagnostik aus (Werte > 444 ng/ml gelten als Risikofaktor), welcher akute, kardiovaskuläre Krankheiten bereits in einem frühen Stadium anzeigen als Wert zur Prognoseabschätzung sowie in der Vorsorge zur Identifizierung von Risikopatienten eingesetzt werden kann. Artherosklerotische Plaques der Gefäßwand mit erhöhtem Komplikationsrisiko weisen große Mengen an Entzündungszellen (Neutrophile, Makrophagen) auf, welche das als Alarmin fungierende heterodimere Protein Calprotectin (S100A8/A9) ausscheiden. Aus diesem Grund werden bei Patienten mit Arteriosklerose durschnittlich signifikant erhöhte Konzentrationen an Calprotectin im Serum nachgewiesen. Calprotectin dient als aktiver Mediator in der Pathogenese atherosklerotischer Läsionen, da die Bindung des Moleküls an Gefäßendothelzellen die Bildung proinflammatorischer Zytokine und die Expression von Adhäsionsmolekülen induziert, das wiederum zur Förderung entzündlicher und thrombogener Prozesse in den Gefäßen führt. Deutlich erhöhte Werte von Calprotection im Serum werden außerdem noch in Patientengruppen mit Herzinfarkt, Schlaganfall und Thrombosen gefunden, da atherosklerotische Prozesse starke Risikofaktoren für kardiovaskuläre Erkrankungen darstellen. Des Weiteren können andere Parameter in dazugehörigen Profilen sowie ein Mikronährstoff-Status des Patienten erhoben werden, um das kardiovaskuläre Risiko zu ermitteln. |
| Lifestyle-Empfehlungen |
|
In der Therapie der KHK stehen die Linderung von Beschwerden, sowie die positive Beeinflussung des Verlaufs im Vordergrund. Dabei liegt der Fokus vor allem auf der Änderung des Lebensstils, der Kontrolle von Risikofaktoren, der Medikamenteneinnahme, so wie den Maßnahmen zur Verbesserung des Blutflusses in den Herzkrankgefäßen. Um dem Fortschreiten der Artherosklerose entgegen zu wirken und in weiterer Folge die Gefahr von ernsten Komplikationen wie Herzinfarkt, Herzschwäche und Herzrythmusstörungen zu unterbinden, zeigt sich die Wichtigkeit, die Risikofaktoren der KHK so weit es geht auszuschalten. Die American Heart Association hat in diesem Zusammenhang 7 Grundregeln aufgestellt, welche Herz-Kreislauf-Erkrankungen vorbeugen sollen („Life’s Simple 7“), darunter: |
| Relevante Mikronährstoffe |
|
Ein wichtiger Punkt in der Prävention von KHK ist das Halten eines gesunden Gewichts mit dem Verlangen nach Süßem abschwächen und Appetit zu dämpfen.Bei Psyllium (Flohsamenschalen) handelt es sich um einen stark quellenden Ballaststoff. Psyllium kann begleitend therapeutisch Maßnahmen zur Gewichtskontrolle unterstützen, indem es rasch wiederaufflammendem Hunger und Appetit entgegenwirkt. Ballaststoffe beginnen bereits im Magen zu quellen, wodurch das Speisebreivolumen ansteigt. Das Resultat ist ein lang anhaltender Sättigungseffekt, der das Einsetzen eines erneuten Hungergefühls verzögert. Durch die modulierte Insulinausschüttung kommt es zudem auch auf Stoffwechselebene zu geringeren Appetit- und Hungersignalen. Auch die Aminosäuren 5-Hydroxytryptophan, L-Tryptophan und L-Phenylalanin dämpfen das Hungergefühl und L-Glutamin mindert das Verlangen nach Kohlenhydraten.
Den Blutdruck niedrig zu halten und somit die Endothelzellen zu schüzten, stellt einen wichtigen Faktor in der Prävention von KHK dar. Sekundäre Pflanzenstoffe, wie die oligomeren Proanthocyanidine (OPC), verbessern die Endothelfunktionen, indem sie die Synthese des gasförmigen Neurotransmitters NO (Stickstoffmonoxid) erhöhen. NO hat eine Schlüsselfunktion bei der Regulierung des Gefäßtonus. Es bewirkt an den Rezeptoren der Gefäßmuskulatur eine Muskelrelaxation, wodurch es in der Folge zu einer Vasodilatation kommt. Besonders OPC-reich sind Traubenkerne und der Pinienrindenextrakt Pycnogenol®. Zudem verhindert OPC arteriosklerosefördernde Ereignisse bereits in der Frühphase, indem oxidative Gefäßschädigungen vermieden werden können. Außerdem wird OPC aufgrund seiner antiödematösen, antiphlogistischen und antioxidativen Fähigkeiten zur therapeutischen Behandlung von Bindegewebsschwächen und begleitend therapeutisch in den Anfangsphasen venöser Erkrankungen eingesetzt. OPC erhöht die Kapillardurchblutung und normalisiert die gestörte Gefäßdurchlässigkeit. Es bringt die überdehnten Venen wieder auf ihren normalen Durchschnitt und hilft beim Abbau von Flüssigkeitsansammlungen im Gewebe. Zudem kann OPC die feinen Gefäßwände und das umgebende Bindegewebe vor altersbedingten oxidativen Prozessen schützen. Im Zusammenhang mit normalen Blutspiegeln und dem Managment von Diabetes mellitus haben die Spurenelemente Selen und Chrom nachgewiesene insulinmimetische Eigenschaften. Die Spurenelemente Selen und Chrom haben nachgewiesene insulinmimetische Eigenschaften. Zu ihren Aktivitäten zählen die Stimulierung der Glukoseaufnahme, die Regulation der Glykolyse sowie die Fettsäuresynthese. Als zugrunde liegender Mechanismus wurde für das Selen eine gesteigerte Phosphorylierung einzelner Schlüsselproteine beschrieben, wodurch das Selen steuernd in die Insulinsignalkaskade eingreift. Dreiwertiges Chrom scheint über die Cholesterolhomöostase in den Zellmembranen auf die Glukoseverwertung regulierend einzuwirken. Die Substitution von Zink kann einen erniedrigten Zinkspiegel beim Diabetiker normalisieren, zu einer verbesserten glykämischen Kontrolle führen und vor diabetesinduzierten Kardiomyopathien schützen. Der Verzicht auf Zigaretten ist wichtig um oxidative Schädigung zu vermeiden. Wenn es nicht möglich ist, das Rauchen aufzugeben, sollten ausreichend hohe Antioxidantienspiegel erreicht werden, um Schäden, die durch die zusätzliche oxidative Belastung verursacht werden, zu vermeiden. Abgesehen vom Einsatz bei Rauchern, konnten epidemiologische Studien den Zusammenhang zwischen unzureichender Versorgung mit Antioxidantien und dem Auftreten von arteriosklerotischen Veränderungen bestätigen. Vor allem für die Vitamin-C-, Vitamin-E- und Beta-Carotin-Zufuhr liegen eindeutige Ergebnisse vor. Diese antioxidativen Systeme vermindern die Oxidation des LDL-Cholesterols zu toxischem ox-LDL, verhindern Lipidperoxidationen und Membranveränderungen und scheinen über eine Verminderung entzündungsfördernder Zytokine arteriosklerotischen Vorfällen entgegenzuwirken. Weitere orthomolekulare Maßnahmen zur Prävention und Therapiebegleitung koronarer Herzkrankheiten stellen die Kontrolle des Homocysteinspiegels, die Erhöhung des Vitamin-D-Spiegels, die Stärkung der Herzmuskulatur, die Verbesserung der Herzleistung, die Reduzierung der Nebenwirkung von Statinen sowie die Minderung des Thromboserisikos dar. Ein erhöhter Homocysteinspiegel gilt als unabhängiger Risikofaktor für Herz-Kreislauf-Erkrankungen und verschärft zusätzlich die Gefahr arteriosklerotischer Veränderungen. Vitamin B6, Vitamin B12 und Folsäure tragen zur Normalisierung des Homocysteinstoffwechsels bei und reduzieren das Fortschreiten einer Folgeerkrankung. Vitamin D3 wirkt regulierend auf die myokardiale Calciumhomöostase, auf die Leistung des Herzmuskels sowie auf den Blutdruck. Verschiedene Studien dokumentieren eine inverse Korrelation zwischen dem Vitamin-D3-Spiegel und der kardiovaskulären Mortalität. In einer groß angelegten Querschnittsstudie war ein Vitamin-D-Defizit im Vergleich zu einem guten Status (Calcidiol größer gleich 75 nmol/l) mit einem 2,8-fach erhöhten Risiko für Tod durch Herzversagen und einem 5-fach erhöhten Risiko für einen plötzlichen Herztod assoziiert. |